君实生物:年轻创新药企突遇“成长考验” 踏出舒适圈直面严峻挑战
近年来,年轻的创新药企,伴随着医药行业创新势头的高涨和一系列药政改革的有力助推,实现了雨后春笋般的新生和加速发展。
但是,此前尚未经历过重大公共卫生事件的年轻药企,此次,面对情形严峻、波及范围广泛的疫情爆发,缺乏更多企业往常经验的借鉴,第一次,开始探索解决方案,寻找突破路径。冲击之下,种种挑战一并而至,面对考验和历练,一场加速成长正在进行,能否调整步伐恢复奔跑,结果拭目以待。

生产车间内景
开拓更多新领域,突破热门赛道
在抗疫战场上,具备创新研发实力的药企正尝试不同路径研发创新,瞄准方向和切入赛道不同,而进入方法亦是各有差异,自主研发、老药新用、投资合作,各不相同。事实上,从自身优势和瞄准赛道出发的创新研发,背后更有着眼疫情过后,对未来产品线扩充和拓展的考虑。
根据君实生物2月3日发布的公告显示,公司拟出资1000万元参与斯微生物A+轮融资,并获得其2.86%的股权。据悉,斯微生物是国内较早开展mRNA药物研发生产的平台型企业。针对本次疫情,斯微生物与中国疾控中心、上海同济大学医学院共同设计开发新冠病毒疫苗,该疫苗基于mRNA平台开发,目前正处于动物试验阶段,预计4月可进入临床研究。
据了解,作为新型疫苗研发技术,mRNA疫苗临床前研究周期较短、产业化难度低,在应对突发传染病上有一定优势。此外,君实生物CEO李宁告诉财经网产经,“此次,公司与斯微生物合作,更看中其在mRNA药物研发生产方面的平台优势。未来,对于公司抗肿瘤、治疗心脑血管疾病的药物产品线补充会有更多帮助。”他透露,通过mRNA平台,公司未来将定制更多产品,与现有产品线实现互补。
而此次尝试与mRNA平台合作,探索不同方向,也有君实生物在此次突发状况下,对近年来创新医药行业的复盘和思考,“当下本土创新药领域,热门赛道拥挤热闹,但抗病毒、抗感染领域较少涉及,创新药企面对突发状况准备不足,确实会感到猝不及防”,李宁谈到,“以往,很多创新药企业最先考虑的是短期的成功,然后再考虑长期发展,但是通过这次疫情,大家的眼光会放得更长远。”
目前,君实生物进入商业化供药的产品为抗肿瘤药物特瑞普利单抗(商品名:拓益),据公司不久前公布的数据显示,该款产品2019年全年实现销售收入7.74亿,君实生物也在此前接受财经网产经采访时谈到,公司的特瑞普利单抗受到关注,正是因为它是首要针对国内患者,且最早得到良好结果的本土创新PD-1。但不得不直面的是,截至目前,这一赛道国内外已有多家企业进入,此外,更有后来者不断入局。
而对于如何在疫情下,尽可能降低上市产品在商业化方面所受的冲击,君实生物采取了多种措施。李宁介绍道,为保证节后正常供货,生产基地在春节期间灵活协调,尽可能用最少的人力完成适当放缓后的生产计划。由于不少省份的航路、公路等物流通道暂时关停,针对航路不畅的路线,将空运调整为货车运输;而针对白天封路的路线,物流司机在晚上也加班工作。对于一些疫情防控的重点地区,不少药房、药品注射点关闭,公司整合了全城至临近城市的药房、注射点信息,供医生和患者了解。
“疫情比较严重的地区,影响不可避免,不过从整体上看,预估疫情对一季度销售业绩的影响不会太明显。去年以来,公司在销售队伍的规模、覆盖的医院广度方面都在不断扩大,相应地会在其他省份地区带来一定的业绩增长。此外,公司在这次疫情中还尝试了多种线上的医学教育方式,也看到了创新的医学推广模式带来的效果。”李宁补充道,随着疫情过去,新适应症的上市递交工作再次提上日程,公司将在近期递交特瑞普利单抗两项新适应的上市申请鼻咽癌和尿路上皮癌,有望在今年年底或明年年初获批,也将有助于公司进一步打开市场。
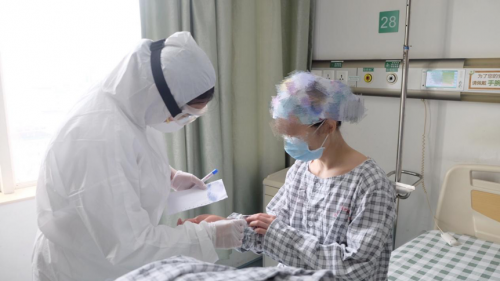
临床患者受试用药(研究者供图)
平衡布局多中心,减缓突发冲击
此次突发疫情对于创新药企而言,无疑在创新药物研发和临床研究方面遭遇巨大挑战,首当其冲的便是临床试验入组、受试者用药、随访及现场监察等环节,能否按照原有临床试验方案实施,确保方案不偏离,药物研发工作正常展开,任务艰巨。
据君实生物科创板提交的招股书显示,公司目前在研管线中,有4大病种、13个在药物、23个适应症处于开发阶段,其中有5个生物药品正在临床阶段,8个处于临床前研究。
特殊情况下,若药物研发和临床研究困境无解,将意味着企业和患者都会面临巨大“风险”和“危机”。此前,君实生物方面就曾表示,有些临床研究已经完成入组,正处在随访阶段,如果病人长时间不能完成规范的访视,研究者就无法及时获取病人的相关信息和情况,无法安排后续治疗;还有一些受试者新入组,多数正处于标准治疗的初始阶段,如果因为疫情中断临床试验的治疗,对受试者而言从所参与临床研究中得到获益将受到影响,疗效无法保障。
关于公司为此所做的努力,李宁对财经网产经介绍道,近段时间以来,公司协调医院伦理、机构、CRO、SMO等临床试验相关方,探讨解决方案,对于部分无法在原临床试验机构继续接受访视和治疗的受试者,按照GCP原则要求,在受试者充分知情同意的前提下,协调资源帮助受试者进行转移,保障受试者权益。
为保证受试者、研究者以及其他参与临床研究人员的安全,公司派出研究团队,协调可利用的医院资源,尽力保证受试者的持续用药和随访。不仅如此,为了减少研究者、受试者和合作方感染新冠肺炎的风险,公司还提供了大量免费的防护用具,主动安排病患单独的交通工具。此外,公司亦与药监部门沟通,调整研究方案,改变研究策略,妥善安排患者,得到了药监部门的支持。
疫情期间,需要解决和应对的难题每天都在发生,君实生物方面举例,公司转移的第一例受试者,临床研究协调员全程陪同,提前预约好床位和检查,专门租车,带病人进入医院,确保接收患者的医疗机构严格按照研究方案做好药物输注、病案记录。而在疫情最严峻的时期,有受试者第二天需要用药,正值春节,物流公司无法即刻送达,患者等不及,公司安排员工,乘坐高铁从北京前往苏州,当天来回专程把试验药物送到受试者就诊的医疗机构。
经历了突发状况下临床研究难题的紧急处理,在李宁看来,“更全面、平衡的布局”能够让企业更从容地应对突发事件。“公司开展的鼻咽癌国际多中心临床研究目前已完成患者入组,当国内形势比较严峻的时候,东南亚地区的试验相较平稳推进。”他坦言,经过这次疫情,公司对未来战略也有了一定考量,“比如对产品管线的优先级、市场布局等进行调整,进一步增强在海外其他国家和地区地生产、营销、权益引进/转让等方面地合作。”












